Posted by : Slamats
Senin, 19 November 2012
Nama : Slamat
Nim : A1C109019 – (PN)
Jawaban MID SEMESTER Kimia Organik I.
Soal no.1 dan no.2
ALKOHOL
<1.a). Mengapa alkohol sukar disubtitusi oleh gugus lain?
Jawab:
Karena gugus –OH pada alkohol ini merupakan Nukleufil yang kuat, sehingga untuk mensubtitusinya dengan gugus lain sangatlah susah.
Sebagai nukleufil kuat, gugus –OH akan mengikat atom Karbon (C) dengan sangat kuat, Sehingga akan susah untuk disubtitusi dengan gugus lain yang nukleufil lebih lemah dari –OH.
b). Jelaskan bagaimana upaya yang dilakukan agar dapat disubtitusi oleh gugus lain.
Jawab:
Upaya yang dilakukan agar gugus –OH dapat disubtitusi yaitu:
Mensubtitusi –OH dengan Nukleufil yang lebih kuat dalam suasana asam.
Misalnya: F,Cl,Br
ALAKNA
<2. a). Mengapa alkana sukar bereaksi dengan senyawa lain?
Jawab:
Karena alkana merupakan hidrokarbon jenuh yang bersifat kurang reaktif, yang hanya memiliki ikatan tunggal antara C-C dan C-H. Seperti yang diketahui pada alkana ini terdapat ikatan antara C-H yang sangat sukar bereaksi.
Alkana ini memiliki rumus umum CnH2n+2, maka semakin panjang rantai alkana akan semakin semakin sukar untuk bereaksi dikarenakan pada alkana tersebut semakin jenuh.
b). Jelaskan bagaimana upaya yang dilakukan agar alkana dapat bereaksi dengan yang lain?
Jawab:
Upaya yang dilakukan agar alkana dapat bereaksi dengan yang lain yaitu:
Cara 1
Melakukan Cracking pada alkana rantai panjang. Cracking itu sendiri adalah proses pemutusan ikatan alkana rantai panjang menjadi alkana yang memiliki rantai-rantai yang lebih pendek ( C5-C10). Dengan semakin pendek rantai alkana maka kejenuhan alkana berkurang, dengan berkurangnya derajat kejenuhan alkana maka alkana akan mudah bereaksi dengan kecenderungan bereaksi melalui radikal bebas.
Contoh:
Cara 2
Membentuk alkena dengan cara dehidrogenesasi sehingga merubah senyawa alkana yang bersifat jenuh menjadi senyawa alkena yang bersifat tak jenuh sehingga mudah bereaksi dengan senyawa lain.
Contoh:
Cara 3
cara lain yaitu dengan mereaksikan dengan halogen yang notabene merupakan nukleufill kuat dengan urutan F > Cl > Br > I












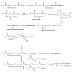





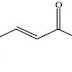



saya akan mencoba mengomentari postingan anda:saya kurang setuju dengan anda karena menurut saya alkohol itu bisa disubstitusi dengan gugus fungsi lainnya.alkohol bisa disubstitusi dengan halogen.contoh reaksi alkohol dengan fosfor halida
BalasHapusUntuk reaksi yang melibatkan fosfor halida, alkohol biasanya dipanaskan dibawah refluks dengan campuran fosfor merah dengan bromin atau iodin, bukan fosfor(III) bromida atau iodida yang digunakan.Fosfor pertama-tama bereaksi dengan bromin atau iodin menghasilkan fosfor(III) halida.
untuk soal no 2 saya setuju dengan postingan anda.Dimana kita tahu semakin panjang rantai alkana makin sukar juga bereaksi karena sifat kejenuhan dari alkana tadi.
saya akan mencoba menyanggah postingan anda
BalasHapusSelain itu dapat juga dilakukan dehidrasi etanol menghasilkan etena
Cara ini merupakan sebuah cara yang sederhana untuk membuat alkena berwujud gas seperti etena. Jika uap etanol dilewatkan di atas bubuk aluminium oksida yang dipanaskan, maka etanol akan terpecah menghasilkan etena dan uap air.
Reaksinya adalah
Setelah menjadi alkena, dapat disubsitusi oleh senyawa lain seperti F, Br, Cl.
Untuk upaya mensubsitusi alkana dapat juga dilakukan melalui reaksi pembakaran.
Saya setuju dengan jawaban ini , dan saya hanya ingin menambahkan jawaban saudara.Alkana (juga disebut dengan parafin) adalah senyawa kimia hidrokarbon jenuh asiklis. Alkana termasuk senyawa alifatik. Dengan kata lain, alkana adalah sebuah rantai karbon panjang dengan ikatan-ikatan tunggal. Rumus umum untuk alkana adalah CnH2n+2. Alkana yang paling sederhana adalah metana dengan rumus CH4. Tidak ada batasan berapa karbon yang dapat terikat bersama. Beberapa jenis minyak dan wax adalah contoh alkana dengan atom jumlah atom karbon yang besar, bisa lebih dari 10 atom karbon.
BalasHapusSetiap atom karbon mempunyai 4 ikatan (baik ikatan C-H atau ikatan C-C), dan setiap atom hidrogen mesti berikatan dengan atom karbon (ikatan H-C). Sebuah kumpulan dari atom karbon yang terangkai disebut juga dengan rumus kerangka. Secara umum, jumlah atom karbon digunakan untuk mengukur berapa besar ukuran alkana tersebut (contohnya: C2-alkana).