Posted by : Slamats
Selasa, 16 Oktober 2012
Kalkon
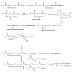
Struktur Kalkon :
 Senyawa kalkon merupakan salah satu senyawa flavonoid, yaitu senyawa yang kerangka karbonnya terdiri atas gugus C6-C3-C6. Strukturnya dapat dibedakan dari senyawa flavonoid lain dari cincin C3 yang terbuka (Gambar 1). Kalkon adalah aglikon flavonoid yang pertama kali terbentuk dalam biosintesis semua varian flavonoid melalui jalur prazat dari alur ‘siklamat’ dan alur ‘asetat malonat’ (Markham, 1998). Kalkon umumnya terdapat dalam tanaman yang termasuk keluargaHeliantheaetribe, Coreopsidinae, dan Compositae (Sastrohamidjojo, 1996).
Senyawa kalkon merupakan salah satu senyawa flavonoid, yaitu senyawa yang kerangka karbonnya terdiri atas gugus C6-C3-C6. Strukturnya dapat dibedakan dari senyawa flavonoid lain dari cincin C3 yang terbuka (Gambar 1). Kalkon adalah aglikon flavonoid yang pertama kali terbentuk dalam biosintesis semua varian flavonoid melalui jalur prazat dari alur ‘siklamat’ dan alur ‘asetat malonat’ (Markham, 1998). Kalkon umumnya terdapat dalam tanaman yang termasuk keluargaHeliantheaetribe, Coreopsidinae, dan Compositae (Sastrohamidjojo, 1996).
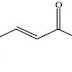
Pada struktur senyawa kalkon, subtituen pada 2 cincin aromatis yang mengapit enon akan memberikan pengaruh terhadap elektrofilisitas struktur enon melalui peningkatan ataupun penurunan kerapatan elektron pada cincin aromatis. Adanya gugus pemberi elektron akan menurunkan elektrofilisitas dari cincin enon. Demikian pula sebaliknya, adanya gugus penarik elektron pada cincin c aromatis akan meningkatkan aktivitasnya sebagai agen pengalkil nukleofil biologis dalam biosintesis IL-1 sebagai antiinflamasi (Batt dkk, 1993).
Senyawa kalkon memiliki aktivitas inhibisi angiogenesis melalui adisi nukleofilik pada gugus enon (Robinson dkk, 2003). Menurut Batt dkk (1993), jembatan enon pada senyawa 2’-kalkon tersubtitusi memegang peranan penting dalam mekanisme aksi inhibitor biosintesis IL-1 karena dapat berperan sebagai agen elektrofilik pengalkilasi. Para agen pengalkilasi memberikan efek sitotoksik melalui transfer alkyl group untuk berbagai konstituen seluler. Alkilasi DNA dalam inti atom mungkin mewakili interaksi utama yang menyebabkan kematian sel (Katzung, 2006).
Senyawa pengalkilasi dapat membentuk senyawa kationik antara yang tidak stabil, diikuti pemecahan cincin membentuk ion karbonium reaktif. Ion ini bereaksi, melalui reaksi alkilasi, membentuk ikatan kovalen dengan gugus-gugus donor elektron, seperti gugus-gugus karboksilat, amin, fosfat, dan tiol, yang terdapat pada struktur asam amino, asam nukleat dan protein, yang sangat dibutuhkan untuk proses biosintesis sel. Reaksi ini membentuk hubungan melintang (cross-lingking) antara dua rangkaian DNA dan mencegah mitosis. Akibatnya proses pembentukan sel terganggu dan terjadi hambatan pertumbuhan sel kanker (Siswandono dan Soekardjo, 2000)
Isolasi
Banyak senyawa dari golongan ini yang mudah larut dalam air, terutama bentuk glikosidanya, dan oleh karena itu senyawa ini berada dalam ekstrak air tumbuhan, bahkan senyawa yang hanya sedikit larut dalam air kepolarannya memadai untuk diekstraksi dengan baik memakai methanol, etanol atau aseton dan methanol 80% merupakan pelarut yang sering dipakai untuk ektraksi flavonoid. Pengekstraksian kembali larutan dalam air dengan pelarut organik yang tidak bercampur dengan air tetapi agak polar sering kali bermanfaat untuk memisahkan golongan ini dari senyawa yang lebih polar seperti karbohidrat.
Banyak senyawa dari golongan ini yang mudah larut dalam air, terutama bentuk glikosidanya, dan oleh karena itu senyawa ini berada dalam ekstrak air tumbuhan, bahkan senyawa yang hanya sedikit larut dalam air kepolarannya memadai untuk diekstraksi dengan baik memakai methanol, etanol atau aseton dan methanol 80% merupakan pelarut yang sering dipakai untuk ektraksi flavonoid. Pengekstraksian kembali larutan dalam air dengan pelarut organik yang tidak bercampur dengan air tetapi agak polar sering kali bermanfaat untuk memisahkan golongan ini dari senyawa yang lebih polar seperti karbohidrat.
Etil asetat merupakan pelarut yang baik untuk menangani katekin dan proantosianidin.
Benzena dapat dipakai untuk benzofenon dan stilbutena. Amil alkohol dipakai untuk antosianin.
Butyl alkohol sekunder adalah alkohol yang paling polar yang bercampur dengan air secara tidak sempurna, dan jika ekstrak air dijenuhkan dengan natrium klorida atau magnesium sulfat, pelarut ini sangat baik untuk untuk mengekstraksi senyawa golongan ini.
Dari segi analisis masa lampau, berbagai pereaksi pengendap telah digunakan untuk senyawa ini. Timbel asetat netral atatu basa terutama dianjurkan. Flavonoid dapat dibebaskan dari endapan timbel dengan menambahkan asam sulfat encer atau hydrogen sulfide, timbel mengendap sebagai timbel sulfat atau timbel sulfide. Pereaksi lainnya adalah asam pikrat, kalium asetat, barium hidroksida, piridina, iterbium asetat dan sebagainya.
Kromatografi partisi kolom telah digunakan untuk pemisahan senyawa ini, misalnya kolom magnesol atau asam silikat dengan pengelusi etil asetat yang dijenuhkn dengan air atau eter. Alumina terutama berguna dalam pemisahan antosianin yang hanya mempunyai 1 gugus hidroksil bebas pada cincin B dari antosianin yang mengandung 1 atau lebih gugus itu.
Kolom partisi memakai serbuk selulosa digunakan untuk berbagai polifenol, termasuk antosianin. Kromatografi penukar ion berguna untuk pengikatan senyawa aromatik ke kamar berdasr-polistiserena. Beberapa peneliti menganjurkan pemakaian kolom poliamida untuk memurnikan flavonoid.
Daftar Pustaka
- http://jendelafarmasi.blogspot.com/2011/08/senyawa-kalkon_12.html
- Batt dkk, 1993
- Katzung, 2006
- Markham, 1998
- Sastrohamidjojo, 1996
- Siswandono dan Soekardjo, 2000


















asalamu'alaikum wr.wb
BalasHapuskita ketahui bahwa senyawa flavoid contoh nya kalkon dapat menghabat pertumbuhan sel kanker.
setelah membaca artikel ini timbul suatu pertanyaan yaitu:
dari struktur kalkon ini, bagaimana cara jika kita ingin lebih mengaktivasikan kinerja dari kalkon tersebut.?